
|
Experiment des Monats
|
Im Muskel dient Kreatinphosphat als Energiespeicher, aus dem ATP regeneriert werden kann. Kreatinphosphat kann spontan zerfallen, wobei es zu Kreatinin cyclisiert. Kreatinin kann nicht wieder in Kreatin umgewandelt werden und muß daher ausgeschiden werden - Kreatinin gehört zu den harnpflichtigen Stoffen. Über die Nieren werden täglich etwa 1,0-1,5 g Kreatinin ausgeschieden, wobei die Menge proportional zur Muskelmasse ist.
 Leerwert - Probe - Standard |
Geräte:
3 Reagenzgläser, Eppendorf-Pipette mit Pipettenspitzen, Küvetten, Spektralphotometer
Urin-Probe (oder entsprechend verdünnte Kreatinin-Lösung),
Kreatinin-Standard (177 µmol/l)
Enzym-Reagenz 1: Puffer pH 7,5; Kreatin-Amidinohydrolase, Sarkosin-Oxidase, Katalase,
Ascorbat-Oxidase, TOOS (3-(N-Ethyl-3-methylanilino)-2-hydroxypropan-sulfonsäure)
Enzym-Reagenz 2: Puffer pH 7,5; Kreatinin-Amidohydrolase, Peroxidase, PAP (4-Aminoantipyrin)
(Reagenzien z.B. von Merck®, mti-Diagnostics oder Fisher-Scientific®)
Durchführung:
10 µl der Urin-Probe wird mit 200 µl dest. Wasser verdünnt.
Drei Reagenzgläser werden mit je 1 ml des Enzym-Reagenz 1 gefüllt.
Zum ersten Reagenzglas kommen 50 µl Wasser, zum zweiten 50 µl der verdünnten Urin-Probe
in das dritte 50 µl der Kreatinin-Standard-Lösung.
Die Lösungen gut mischen und 10 min. stehen lassen. Anschließend jeweils 0,5 ml des
Enzym-Reagenz 2 zugeben, mischen und 15 min. warten.
Es entsteht ein rötlicher Farbstoff, dessen Konzentration nun spektralphotometrisch bei 546 nm
bestimmt werden kann.
Erklärung:
Die Reaktion erfolgt in mehreren enzymkatalysierten Schritten:
Kreatinin
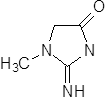 |
+ H2O | Kreatininase
 |
Kreatin
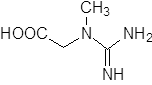 |
|
Kreatin
 |
+ H2O | Kreatinase
 |
Sarkosin
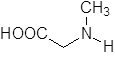 |
+ Harnstoff
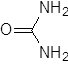 |
Sarkosin
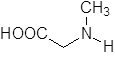 |
+ H2O + O2 | Sarkosinoxidase
 |
Glycin
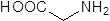 |
+ HCHO + H2O2 |
Zum Schluß wird durch die Peroxidase aus den beiden Farbstoff-Vorstufen PAP und TOOS unter Oxidation durch H2O2 ein roter Farbstoff gebildet. Aus dessen Konzentration kann dann die Kreatinin-Konzentration in der Probe bestimmt werden.
Entsorgung:
Die Lösungen können zum Abwasser gegeben werden.
Literatur & Links:
C. Ludwig, I. Rapoport, U. Kuckelkorn, P. Ludwig: Praktikum Biochemie für Mediziner,
Kurstag Calcium- und Phosphat-Stoffwechsel; Charité - Universitätsmedizin Berlin
Frau Dipl.-Päd. Regina Freund, Institut für Biochemie der Charité, danke ich sehr herzlich für die Unterstützung.
 zurück zum aktuellen Experiment
zurück zum aktuellen Experiment
Seite erstellt am: Dienstag, 1. Juni 2010,
A. Schunk,
Charité - Universitätsmedizin Berlin.
Für den Inhalt externer Seiten wird keine Verantwortung übernommen!