
|
Experiment des Monats
|
Cyclodextrine sind Oligosaccharide aus (meistens) 6-9 Glucose-Molekülen, die zu einem Ring verknüpft sind. Sie sind trotz der Größe gut wasserlöslich, besitzen aber einen eher lipophilen Innenraum, so dass sie unpolare Moleküle einschliessen und damit absorbieren können.
 |
Geräte und Chemikalien:
1%ige alkoholische Phenolphthalein-Lösung,
β-Cyclodextrin,
0,1 M Natronlauge,
Reagenzgläser, Tropfpipette.
Durchführung:
10 ml Natronlauge mit 5 Tropfen Phenolphthalein-Lösung versetzen.
Der Indikator schlägt nach rotviolett um.
0,2 g Cyclodextrin werden in 20 ml Wasser gelöst. In ein zweites
Reagenzglas 20 ml Wasser einfüllen.
Zur Cyclodextrin-Lösung tropfenweise die gefärbte Natronlauge geben,
bis sich eine bleibende schwache Rosafärbung einstellt. Die gleiche Menge
Natronlauge zum Wasser geben; diese Lösung ist intensiv violett gefärbt.
Mit Universalindikatorpapier zeigt sich in beiden Lösungen ein pH > 10 (der
Umschlagbereich für Phenolphthalein liegt bei pH 8,2-9,6).
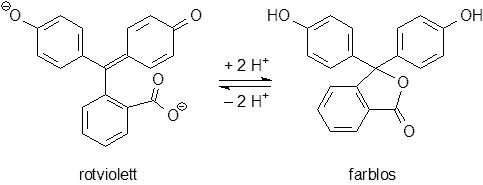 |
Erklärung:
Phenolphthalein liegt in saurer und neutraler Lösung in der farblosen Lacton-Form vor.
In alkalischem Milieu wird der Lacton-Ring gespalten, das Molekül gibt zwei
H
In den Cyclodextrinen kann nur die neutrale Lacton-Form binden. Trotz des hohen pH-Werts
erfolgt daher kein Farbumschlag, so lange die Phenolphthalein-Moleküle weitgehend
"eingefangen" werden. Erst wenn die Kapazität der Cyclodextrine überschritten wird, liegen
genügend frei gelöste Indikator-Moleküle vor, um einen Farbumschlag zu erreichen.
Gefahren:
Natronlauge ist ätzend.
Entsorgung:
Die Lösungen werden neutralisiert und können dann zum Abwasser gegeben werden.
Literatur & Links:
S. Krees, M. Tausch: "Moleküle zu Gast beim Zuckerwirt - Wirt-Gast-Komplexe mit Cyclodextrinen"
Praxis der Naturwissenschaften - Chemie in der Schule, 56 (2007), 33-38
Michael W. Tausch, Simone Krees et al.: Schulversuchskoffer DiSiDo;
Bergische Universität Wuppertal & Wacker Chemie AG, 2007
Dezember 2014: Löslichkeit von Erdalkalisulfaten
 zurück zum aktuellen Experiment
zurück zum aktuellen Experiment
Seite erstellt am: Montag, 5. Januar 2015,
A. Schunk,
Charité - Universitätsmedizin Berlin.
Für den Inhalt externer Seiten wird keine Verantwortung übernommen!